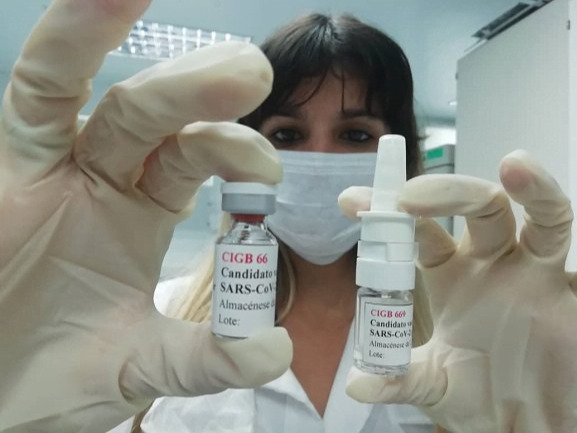
La ciencia cubana da un paso más hacia adelante. Foto: PL
La Habana, 13 jul (RHC) La vacuna antiCovid-19 de Cuba, ‘Abdala’, primera de América Latina y el candidato ‘Mambisa’ se unirán en el segundo ensayo clínico para convalecientes de la Covid-19 en el país, informaron este martes autoridades regulatorias.
Unas 120 personas que hayan padecido la enfermedad estarán incluidos en el estudio fase I/II para evaluar ambos productos, diseñados por el Centro de Ingeniería Genética y Biotecnología de La Habana (CIGB).
De acuerdo con el registro público cubano de estudios clínicos, entre los objetivos de esta etapa está comprobar la inmunogenicidad y funcionalidad de la administración por spray nasal y por gotas del proyecto Mambisa.
Además, trabajarán en identificar, de acuerdo al balance beneficio-riesgo-costo, la variante de administración nasal de ‘Mambisa’ a utilizar en la etapa II del estudio.
Igualmente evaluarán la inmunogenicidad y funcionalidad de la administración intramuscular de ‘Abdala’, también del CIGB, que demostró un 92,28 de eficacia en su esquema de tres dosis. Este proyecto ya recibió el autorizo de uso de emergencia en la nación caribeña.
El estudio en convalecientes con ambos productos, será intervencional, abierto, aleatorizado y no controlado para voluntarios entre 19 y 80 años, que hayan padecido la enfermedad y lleven al menos dos meses de alta.
De acuerdo con el registro público, se espera con este ensayo clínico que el 55 por ciento o más de los sujetos tratados con los dos candidatos vacunales, incrementen en cuatro veces la determinación inicial de los títulos de los anticuerpos específicos contra el virus SARS-CoV-2, patógeno causante de a Covid-19.
Asimismo, prevén que se eleven en al menos un 20 por ciento los títulos de inhibición de unión al receptor ACE2, sin el riesgo de que se observen más de un cinco por ciento de individuos con eventos adversos graves con causalidad consistente con la vacunación.
Previo a dicho ensayo en convalecientes, la nación caribeña inició otro con el candidato vacunal ‘Soberana Plus’, del Instituto Finlay de Vacunas (IFV), con el cual también se busca evaluar la seguridad, reactogenicidad y la inmunogenicidad de una dosis de la propuesta en pacientes recuperados de la enfermedad. (Fuente: PL)

